字节跳动发布Protenix-v1 实现AlphaFold3级别结构预测
•39 阅读•3分钟•前沿
ByteDanceProtenixAlphaFold3PXMeter
•39 阅读•3分钟•前沿
背景
在生物大分子结构预测领域,AlphaFold3的全原子扩散模型被视为技术前沿。字节跳动在2026年2月推出的Protenix-v1,旨在以完全开源的方式复现AF3的核心能力,并在训练数据截止、模型规模和推理预算上与其保持一致。
关键特性
- 全栈开源:代码、预训练权重、MSA流水线以及浏览器交互式Web Server全部在GitHub发布,采用Apache 2.0协议。
- 多模态预测:一次前向即可输出包含蛋白质、DNA/RNA以及小分子配体的全原子3D结构。
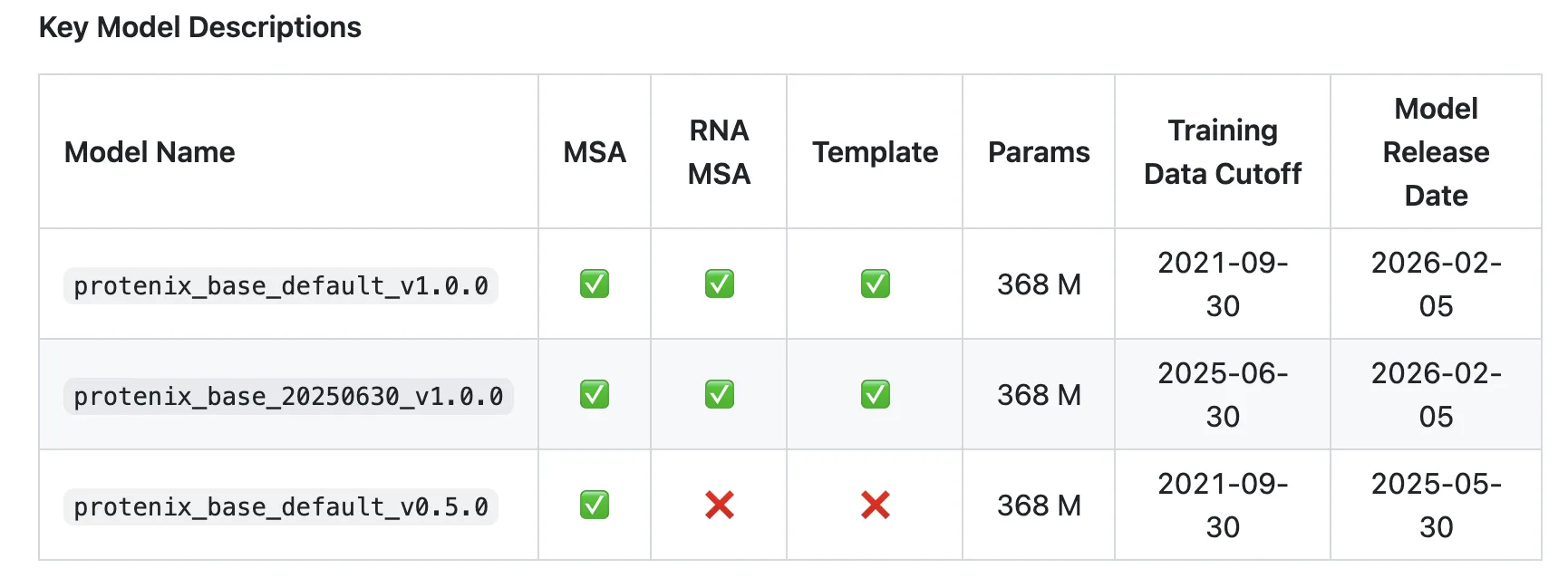
- 模型规模:368M参数的Protenix‑v1在保持AF3级别的模型容量的同时,实现了更易部署的计算需求。
- 推理可扩展:通过增加采样候选数,可实现对复杂抗体‑抗原复合体的对数线性精度提升,提供清晰的延迟‑精度权衡曲线。
基准与评估
Protenix‑v1随同发布的PXMeter v1.0.0提供了6000余个经人工筛选的复合体基准,涵盖时间分割子集、抗体‑抗原、蛋白‑RNA以及配体对接等场景。评测指标包括复合体LDDT、DockQ等,结果显示在所有子集上均超过AlphaFold3的公开基准表现。PXMeter的研究论文进一步阐释了不同数据划分对模型排名的影响,提升了评测的可复现性。
生态与后续
Protenix已衍生出多个配套项目:
- PXDesign:基于Protenix的结合体设计套件,实验命中率提升20%‑73%。
- Protenix‑Dock:传统经验评分的蛋白‑配体对接框架,针对刚性对接进行专门调优。
- Protenix‑Mini 系列:通过架构压缩与少步采样,将推理成本降低数倍,精度损失控制在几个百分点内。
这些组件共享统一的输入输出格式,便于在药物发现、酶工程等下游流水线中直接集成。
"Protenix‑v1 是首个在保持AlphaFold3关键约束下实现全开源、全可复现的高精度结构预测模型。"——字节跳动AI实验室负责人
整体来看,Protenix‑v1不仅在学术前沿提供了可验证的基准,还为工业界提供了落地的工具链,预示着AI驱动的生物结构预测将在开源生态中迎来新一轮加速。
本文是对第三方新闻源的主观解读。消息可能出现过时、不准确、歧义或错误的地方,仅供参考使用。点击此处查看消息源。